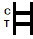Test rapido della fibronectina fetale
Uso ntentato
Il filo®Il test Prom è un test immunocromatografico visivamente interpretato che si intende essere utilizzato per la rilevazione qualitativa della fibronectina fetale nelle secrezioni cervicovaginali. La presenza di fibronectina fetale nelle secrezioni cervicovaginali tra 22 settimane, 0 giorni e 34 settimane, 6 giorni di gestazione èassociato a un elevato rischio di consegna pretermine.
Troduzione
La consegna pretermine, definita dall'American College of Obstetricians and Gynecologists come consegna prima della 37a settimana di gestazione, è responsabile della maggior parte della morbilità e della mortalità perinatale non cromosomica. I sintomi del parto pretermine minacciati comprendono contrazioni uterine, cambio di scarico vaginale, sanguinamento vaginale, mal di schiena, disagio addominale, pressione pelvica e crampi. Le modalità diagnostiche per l'identificazione della consegna pretermine minacciate includono il monitoraggio delle attività uterine e le prestazioni di un esame cervicale digitale, che consente la stima delle dimensioni cervicali. Questi metodi hanno dimostrato di essere limitati, poiché la dilatazione cervicale minima (<3 centimetri) e l'attività uterina si verificano normalmente e non sono necessariamente diagnostiche della consegna pretermine imminente. Mentre sono stati valutati diversi marcatori biochimici sierici, nessuno è stato ampiamente accettato per uso clinico pratico.
La fibronectina fetale (FFN), un'isoforma della fibronectina, è una glicoproteina adesiva complessa con un peso molecolare di circa 500.000 daltons. Matsuura e collaboratori hanno descritto un anticorpo monoclonale chiamato FDC-6, che riconosce specificamente III-CS, la regione che definisce l'isoforma fetale della fibronectina. Gli studi immunoistochimici di placenta hanno dimostrato che FFN èConfinato alla matrice extracellulare della regione che definisce la giunzionedelle unità materne e fetali all'interno dell'utero.
La fibronectina fetale può essere rilevata nelle secrezioni cervicovaginali delle donne durante la gravidanza mediante l'uso di un test immunologico anticorpale monoclonale. La fibronectina fetale è elevata nelle secrezioni cervicovaginali durante la gravidanza precoce ma è ridotta da 22 a 35 settimane in gravidanze normali. Il significato della sua presenza nella vagina durante le prime settimane di gravidanza non è compreso. Tuttavia, può semplicemente riflettere la normale crescita della straordinaria popolazione di trofoblasti e della placenta. Il rilevamento di FFN nelle secrezioni cervicovaginali tra 22 settimane, 0 giorni e 34 settimane, 6 giorni la gestazione è associata alla consegna pretermine in sintomatico e tra 22 settimane, 0 giorni e 30 settimane, 6 giorni in donne in gravidanza asintomatica.
PRINCIPIO
Il filo®Il test FFN utilizza la tecnologia immunocromatografica del colore e capillare. La procedura di prova richiede la solubilizzazione di FFN da un tampone vaginale mescolando il tampone nel tampone del campione. Quindi il tampone del campione misto viene aggiunto al pozzo del campione di cassetta di prova e la miscela migra lungo la superficie della membrana. Se FFN è presente nel campione, formerà un complesso con l'anticorpo anticorpo anticorro primario coniugata a particelle colorate. Il complesso sarà quindi vincolato da un secondo anticorpo anticorpo rivestito sulla membrana di nitrocellulosa. L'aspetto di una linea di prova visibile insieme alla linea di controllo indicherà un risultato positivo.
Componenti del kit
| 20 Individualmente pAckDispositivi di test ED | Ogni dispositivo contiene una striscia con coniugati colorati e reagenti reattivi pre-rivestiti nelle regioni corrispondenti. |
| 2EstrazioneFial tampone | Salino tamponato fosfato 0,1 M (PBS) e 0,02% di sodio azide. |
| 1 tampone di controllo positivo (solo su richiesta) | Contenere FFN e sodio azide. Per controllo esterno. |
| 1 tampone di controllo negativo (solo su richiesta) | Non contenere FFN. Per controllo esterno. |
| 20 Tubi di estrazione | Per l'uso della preparazione dei campioni. |
| 1 Workstation | Posizionare per contenere fiale e tubi tampone. |
| 1 Inserto del pacchetto | Per l'istruzione operativa. |
Materiali richiesti ma non forniti
| Timer | Per l'uso di tempismo. |
PRECAUZIONI
■ Solo per uso diagnostico professionale in vitro.
■ Non utilizzare dopo la data di scadenza indicata sul pacchetto. Non utilizzare il test se la sua custodia per foglio è danneggiata. Non riutilizzare i test.
■ Questo kit contiene prodotti di origine animale. La conoscenza certificata dell'origine e/o dello stato sanitario degli animali non garantisce totalmente l'assenza di agenti patogeni trasmissibili. È quindi raccomandato che questi prodotti siano trattati come potenzialmente contagiosi e gestiti osservando le solite precauzioni di sicurezza (non ingerire o inalare).
■ Evitare la contaminazione incrociata dei campioni utilizzando un nuovo contenitore di raccolta di campioni per ciascun campione ottenuto.
■ Leggere attentamente l'intera procedura prima di eseguire eventuali test.
■ Non mangiare, bere o fumare nell'area in cui vengono gestiti esemplari e kit. Gestisci tutti i campioni come se contengano agenti infettivi. Osservare precauzioni stabilite contro i pericoli microbiologici durante la procedura e seguire le procedure standard per lo smaltimento corretto dei campioni. Indossare indumenti protettivi come cappotti da laboratorio, guanti usa e getta e protezione degli occhi quando vengono analizzati i campioni.
■ Non scambiare o mescolare reagenti da lotti diversi. Non mescolare i tappi della bottiglia di soluzione.
■ L'umidità e la temperatura possono influenzare negativamente i risultati.
■ Quando la procedura del dosaggio è completata, smaltire i tamponi attentamente dopo averli autoclay a 121 ° C per almeno 20 minuti. In alternativa, possono essere trattati con lo 0,5% di ipocloruro di sodio (o candeggina in casa) per un'ora prima dello smaltimento. I materiali di test utilizzati devono essere scartati in conformità con le normative locali, statali e/o federali.
■ Non utilizzare i pennelli citologici con pazienti in gravidanza.
Archiviazione e stabilità
■ Il kit deve essere conservato a 2-30 ° C fino alla data di scadenza stampata sulla custodia sigillata.
■ Il test deve rimanere nella custodia sigillata fino all'uso.
■ Non congelare.
■ Le cure devono essere prese per proteggere i componenti in questo kit dalla contaminazione. Non utilizzare se ci sono prove di contaminazione microbica o precipitazione. La contaminazione biologica di attrezzature di erogazione, contenitori o reagenti può portare a risultati falsi.
PECIMEN RACCOLTUZIONE E PROGETTAZIONE
■ Utilizzare solo tamponi sterili con punta di dacron o rayon con alberi di plastica. Si consiglia di utilizzare il tampone fornito dal produttore dei kit (i tamponi non sono contenuti in questo kit, per le informazioni di ordinazione, si prega di contattare il produttore o il distributore locale, il numero del catalogo è 207000). I tamponi di altri fornitori non sono stati validati. Non sono consigliati tamponi con punte di cotone o alberi di legno.
■ Secrezioni cervicovaginali sono ottenute dalla Fornix posteriore della vagina. Il processo di raccolta è destinato a essere delicato. Non è necessaria una raccolta vigorosa o forte, comune per le culture microbiologiche. Durante un esame di speculum, prima di qualsiasi esame o manipolazione della cervice o del tratto vaginale, ruota leggermente la punta dell'applicatore attraverso la fornix posteriore della vagina per circa 10 secondi per assorbire le secrezioni cervicovaginali. I successivi tentativi di saturare la punta dell'applicatore possono invalidare il test. Rimuovere l'applicatore ed eseguire il test come indicato di seguito.
■ Mettere il tampone sul tubo di estrazione, se il test può essere eseguito immediatamente. Se non sono possibili test immediati, i campioni del paziente devono essere collocati in una provetta di trasporto a secco per lo stoccaggio o il trasporto. I tamponi possono essere conservati per 24 ore a temperatura ambiente (15-30 ° C) o 1 settimana a 4 ° C o non più di 6 mesi a -20 ° C. Tutti i campioni dovrebbero essere autorizzati a raggiungere una temperatura ambiente di 15-30 ° C prima del test.
PROCEDURA
Portare test, campioni, tampone e/o controlli a temperatura ambiente (15-30 ° C) prima dell'uso.
■ Posizionare un tubo di estrazione pulito nell'area designata della workstation. Aggiungi 1 ml di tampone di estrazione al tubo di estrazione.
■ Mettere il tampone del campione nel tubo. Mescolare vigorosamente la soluzione ruotando con forza il tampone contro il lato del tubo per meno dieci volte (mentre è immerso). I migliori risultati si ottengono quando il campione viene miscelato vigorosamente nella soluzione.
■ Stringi più liquido possibile dal tampone pizzicando il lato del tubo di estrazione flessibile quando il tampone viene rimosso. Almeno 1/2 della soluzione tampone del campione deve rimanere nel tubo per la migrazione capillare adeguata. Metti il cappuccio sul tubo estratto.
Scartare il tampone in un adatto contenitore di rifiuti biohazardo.
■ I campioni estratti possono trattenere a temperatura ambiente per 60 minuti senza influire sul risultato del test.
■ Rimuovere il test dalla custodia sigillata e posizionarlo su una superficie pulita e di livello. Etichettare il dispositivo con il paziente o l'identificazione del controllo. Per ottenere un risultato migliore, il test dovrebbe essere eseguito entro un'ora.
■ Aggiungi 3 gocce (circa 100 µL) del campione estratto dal tubo di estrazione al pozzo del campione sulla cassetta di prova.
Evita di intrappolare le bolle d'aria nel pozzetto / i del campione e non rilasciare alcuna soluzione nella finestra di osservazione.
Quando il test inizia a funzionare, vedrai il colore muoversi attraverso la membrana.
■ Attendere che appaia la banda colorata. Il risultato dovrebbe essere letto a 5 minuti. Non interpretare il risultato dopo 5 minuti.
Scartare i tubi di prova usati e le cassette di prova in un adeguato contenitore per rifiuti biohazardosi.
Interpretazione dei risultati
| POSITIVORISULTATO:
| Due bande colorate appaiono sulla membrana. Una banda appare nella regione di controllo (C) e un'altra banda appare nella regione di prova (T). |
| NEGATIVORISULTATO:
| Solo una banda colorata appare nella regione di controllo (C). Nessuna banda colorata apparente appare nella regione di prova (T). |
| NON VALIDORISULTATO:
| La banda di controllo non riesce ad apparire. I risultati di qualsiasi test che non hanno prodotto una banda di controllo al momento di lettura specificato devono essere scartati. Si prega di rivedere la procedura e ripetere con un nuovo test. Se il problema persiste, interrompere immediatamente l'uso del kit e contattare il distributore locale. |
NOTA:
1. L'intensità del colore nella regione di prova (T) può variare a seconda della concentrazione di sostanze mirate presenti nel campione. Ma il livello di sostanze non può essere determinato da questo test qualitativo.
2. Volume del campione insufficiente, procedura di funzionamento errata o eseguire test scaduti sono i motivi più probabili per il fallimento della banda di controllo.
Controllo di qualità
■ I controlli procedurali interni sono inclusi nel test. Una banda colorata che appare nella regione di controllo (C) è considerata un controllo procedurale positivo interno. Conferma il volume del campione sufficiente e la corretta tecnica procedurale.
■ I controlli procedurali esterni possono essere forniti (solo su richiesta) nei kit per garantire che i test funzionino correttamente. Inoltre, i controlli possono essere utilizzati per dimostrare le prestazioni adeguate da parte dell'operatore di prova. Per eseguire un test di controllo positivo o negativo, completare i passaggi nella sezione Procedura di prova che tratta il tampone di controllo allo stesso modo di un tampone del campione.
Limitazioni del test
1. Questo test può essere utilizzato solo per il rilevamento qualitativo della fibronectina fetale nelle secrezioni cervicovaginali.
2. I risultati dei test devono essere sempre utilizzati insieme ad altri dati clinici e di laboratorio per la gestione dei pazienti.
3. I campioni devono essere ottenuti prima dell'esame digitale o della manipolazione della cervice. Le manipolazioni della cervice possono portare a risultati falsi positivi.
4. I campioni non devono essere raccolti se il paziente ha avuto rapporti sessuali entro 24 ore per eliminare i risultati falsi positivi.
5. I pazienti con abruzione placentare sospetta o nota, placenta previa o sanguinamento vaginale moderato o lordo non devono essere testati.
6. I pazienti con cerclage non devono essere testati.
7. Le caratteristiche prestazionali del Strongstep®Il test FFN si basa su studi su donne con gestazioni singleton. Le prestazioni non sono state verificate su pazienti con gestazioni multiple, ad es. Gemelli.
8. Il Strongstep®Il test FFN non è destinato a essere eseguito in presenza di rottura delle membrane amniotiche e la rottura delle membrane amniotiche dovrebbe essere escluso prima di condurre il test.
Caratteristiche delle prestazioni
Tabella: test FFN Strongstep® contro un altro marchio FFN Test
| Sensibilità relativa: 97,96%(89,13%-99,95%)* Specificità relativa: 98,73%(95,50%-99,85%)* Accordo complessivo: 98,55%(95,82%-99,70%)* *Intervallo di confidenza al 95% |
| Un altro marchio |
| ||
| + | - | Totale | |||
| Strongstep®FFn Test | + | 48 | 2 | 50 | |
| - | 1 | 156 | 157 | ||
|
| 49 | 158 | 207 | ||
Sensibilità analitica
La quantità più bassa rilevabile di FFN nel campione estratto è 50 μg/L.
Tra le donne sintomatiche, livelli elevati (≥ 0,050 μg/ml) (1 x 10-7 mmol/L) di FFN tra 24 settimane, 0 giorni e 34 settimane, 6 giorni indicano un aumento del rischio di consegna in ≤ 7 o ≤ 14 giorni da Raccolta campione. Tra le donne asintomatiche, livelli elevati di FFN tra 22 settimane, 0 giorni e 30 settimane, 6 giorni indicano un aumento del rischio di parto in ≤ 34 settimane, 6 giorni di gestazione. Il taglio di 50 μg/L FFN è stato stabilito in uno studio multicentrico condotto per valutare l'associazione tra espressione di fibronectina fetale durante la gravidanza e il parto pretermine.
Sostanze interferenti
È necessario prestare attenzione a non contaminare le secrezioni applicatore o cervicovaginale con lubrificanti, saponi, disinfettanti o creme. Lubrificanti o creme possono interferire fisicamente con l'assorbimento del campione sull'applicatore. SOAP o disinfettanti possono interferire con la reazione anticorpo-antigene.
Le potenziali sostanze interferenti sono state testate a concentrazioni che potrebbero essere ragionevolmente trovate nelle secrezioni cervicovaginali. Le seguenti sostanze non interferiscono nel test quando testate ai livelli indicati.
| Sostanza | Concentrazione | Sostanza | Concentrazione |
| Ampicillina | 1,47 mg/ml | Prostaglandina F2 | a0,033 mg/ml |
| Eritromicina | 0,272 mg/ml | Prostaglandina E2 | 0,033 mg/ml |
| URINE MATERNA 3 ° trimestre | 5% (Vol) | Monistatr (miconazolo) | 0,5 mg/ml |
| Ossitocina | 10 iu/ml | Carmine indaco | 0,232 mg/ml |
| Terbutalina | 3,59 mg/ml | Gentamicina | 0,849 mg/ml |
| Desametasone | 2,50 mg/ml | Gel Betadiner | 10 mg/ml |
| MgSo4•7H2O | 1,49 mg/ml | Cleanser Betadiner | 10 mg/ml |
| Ritodrina | 0,33 mg/ml | Jelly k-yr | 62,5 mg/ml |
| Dermicidolr 2000 | 25,73 mg/ml |
Riferimenti di letteratura
1. American College of Obstetricians and Gynecologists. Lavoro pretermine. Bollettino tecnico, numero 133, ottobre 1989.
2. Creasy RK, Resnick R. Medicina materna e fetale: principi e pratica. Filadelfia: WB Saunders; 1989.
3. Creasy RK, Merkatz IR. Prevenzione della nascita pretermine: opinione clinica. Obstet Gynecol 1990; 76 (Suppl 1): 2S - 4s.
4. Morrison JC. Nascita pretermine: un puzzle degno di essere risolto. Obstet Gynecol 1990; 76 (Suppl 1): 5S-12s.
5. Lockwood CJ, Senyei AE, Dische MR, Casal DC, et al. Fibronectina fetale nelle secrezioni cervicali e vaginali come predittore del parto pretermine. New Engl J Med 1991; 325: 669–74.
Glossario dei simboli
|
| Numero di catalogo |  | Limitazione della temperatura |
 | Consultare le istruzioni per l'uso |
| Codice batch |
 | Dispositivo medico diagnostico in vitro |  | Utilizzare da |
 | Produttore |  | Contiene sufficiente per |
 | Non riutilizzare |  | Rappresentante autorizzato nella comunità europea |
 | CE contrassegnato secondo la direttiva IVD Medical Devices 98/79/EC | ||
Liming Bio-Products Co., Ltd.
N. 12 Huayuan Road, Nanjing, Jiangsu, 210042 PR China.
Tel: (0086) 25 85476723 Fax: (0086) 25 85476387
E-mail:sales@limingbio.com
Sito web: www.limingbio.com
www.stddiagnostics.com
www.stidiagnostics.com
Wellkang Ltd. (www.ce-marking.eu) tel: +44 (20) 79934346
29 Harley St., London Wig 9QR, UK Fax: +44 (20) 76811874
Strongstep® Fetal Fibronectin Rapid Test Device

La consegna pretermine, definita dall'American College of Obstetricians and Gynecologists come consegna prima della 37a settimana di gestazione, è responsabile della maggior parte della morbilità e della mortalità perinatale non cromosomica. I sintomi del parto pretermine minacciati comprendono contrazioni uterine, cambio di scarico vaginale, sanguinamento vaginale, mal di schiena, disagio addominale, pressione pelvica e crampi. Le modalità diagnostiche per l'identificazione della consegna pretermine minacciate includono il monitoraggio delle attività uterine e le prestazioni di un esame cervicale digitale, che consente la stima delle dimensioni cervicali.
Il test rapido della fibronectina fetale Strongstep® è un test immunocromatografico interpretato visivamente destinato a essere utilizzato per la rilevazione qualitativa della fibronectina fetale nelle secrezioni cervicovaginali con le seguenti caratteristiche:
Facile da usare:Procedura in una fase nei test qualitativi
Rapido:Solo 10 minuti richiesti durante lo stesso paziente in visita
Senza attrezzature:Gli ospedali o l'ambiente clinico limitanti possono eseguire questo test
Consegnato:temperatura ambiente (2 ℃ -30 ℃)