Dispositivo di sistema Strongstep per test rapido dell'antigene SARS-CoV-2
Uso previsto
Il dispositivo di sistema Strongstep® per il test rapido dell'antigene SARS-CoV-2 impiega la tecnologia di immunocromatografia per rilevare l'antigene nucleocapside SARS-COV-2 nella saliva umana. Questo test è solo un uso singolo e destinato a SEI: test. Si raccomanda di utilizzare questo test entro 7 giorni dall'esordio dei sintomi, è supportato dalla valutazione delle prestazioni cliniche.
INTRODUZIONE
I nuovi coronavirus appartengono al genere 0. Covid-19 è una malattia infettiva respiratoria acuta. Le persone sono generalmente sensibili. Attualmente, i pazienti infettati dal nuovo coronavirus sono la principale fonte di infezione basata sull'attuale indagine epidemiologica, il periodo di incubazione è da 1 a 14 giorni, per lo più da 3 a 7 giorni. Le manifestazioni principali includono febbre, affaticamento e tosse secca. In alcuni casi si trovano congestione nasale, naso che cola, mal di gola, mialgia e diarrea.
PRINCIPIO
Il dispositivo di sistema Strongstep® per il test dell'antigene SARS-COV-2 impiega test immunocromatografici, questo kit raccoglie campioni di saliva dal bastone di adsorbimento della saliva nella parte anteriore della scheda di prova e i campioni di saliva si spostano in avanti sotto azione capillare. Se il campione contiene un antigene proteico N SARS-COV-2 N viene identificato e legato dagli anticorpi etichettati sulla superficie in lattice per formare un complesso immunitario. Quando il complesso immunitario formato migra nella linea di rilevamento della membrana della fibra di acido nitrico, per identificare gli anticorpi confezionati e formare una linea di rilevamento fucsia (T-LIN), che mostra l'antigene SARS-CoV-2 positivo; Se la linea T non mostra il colore, è un risultato negativo. Un'altra linea sulla membrana in fibra di acido nitrico è ricca di anticorpi di streptavidina come linea di controllo di qualità (linea C), per indicare un processo di test efficace.
PRECAUZIONI
• Questo kit è solo per uso diagnostico in vitro.
• Questo kit può essere somministrato da personale medico o non medico seguendo le istruzioni operative.
• Leggi attentamente le istruzioni prima di eseguire il test.
• Questo prodotto non contiene materiali per la fonte umana.
• Non utilizzare i contenuti del kit dopo la data di scadenza.
• Gestisci tutti i campioni come potenzialmente contagiosi.
• Non fare il reagente di pipetta per bocca e non fumare o mangiare durante l'esecuzione di saggi.
• Indossare guanti durante l'intera procedura.
Archiviazione e stabilità
Le buste sigillate nel kit di prova possono essere conservate tra 2-30 ° C per la durata della durata di conservazione come indicato sulla sacca.
Raccolta e conservazione dei campioni
Il miglior esemplare di saliva dovrebbe essere raccolto al mattino dopo aver appena svegliato. Non mangiare o bere nulla per 30 minuti prima di raccogliere il campione di saliva. Fallo prima di fare un caffè, fare colazione o lavarti i denti - o attendere fino a non aver consumato nulla nei 30 minuti precedenti.
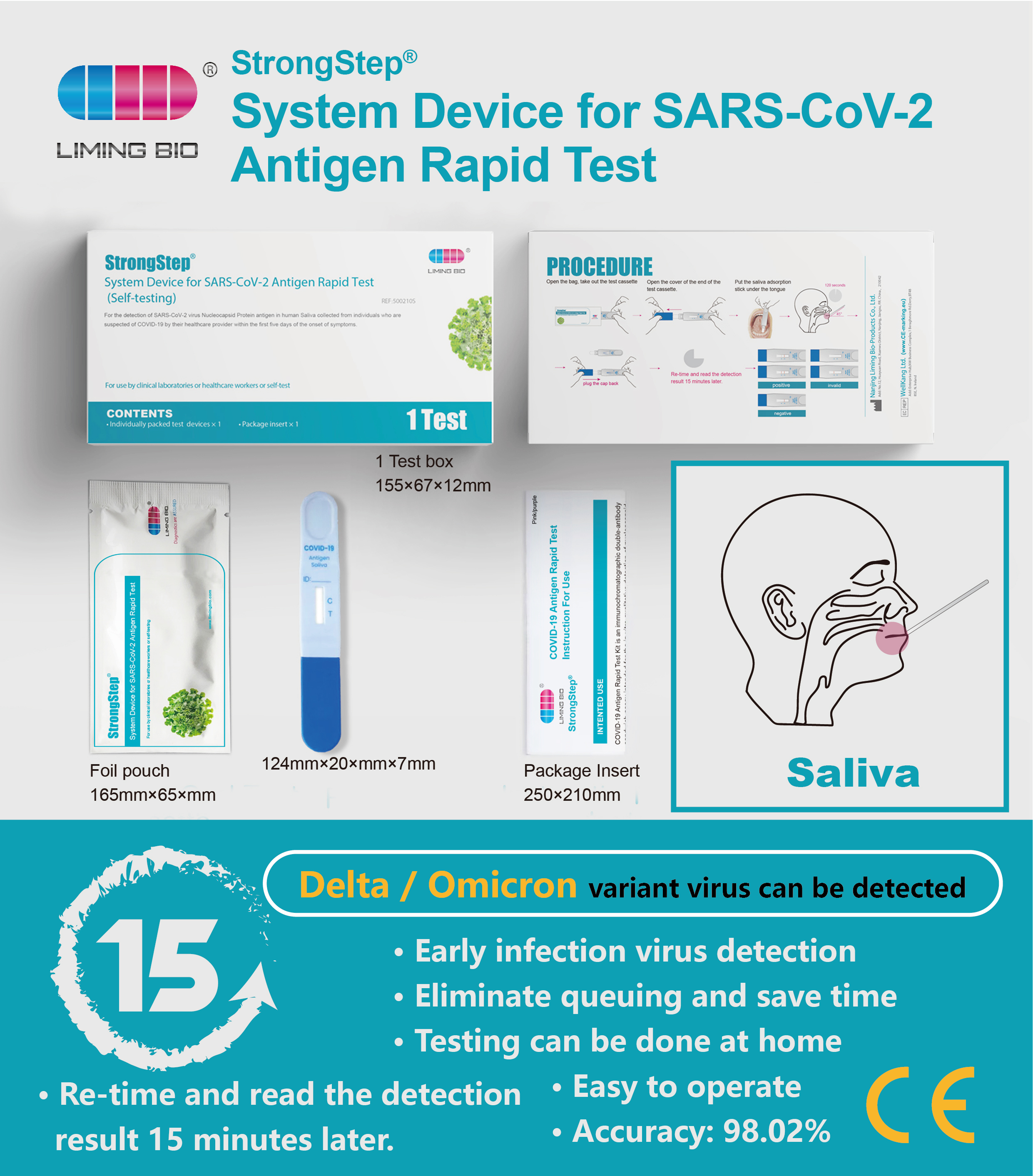
PROCEDURA
Portare i test a temperatura ambiente (15-30 ° C) prima dell'uso.
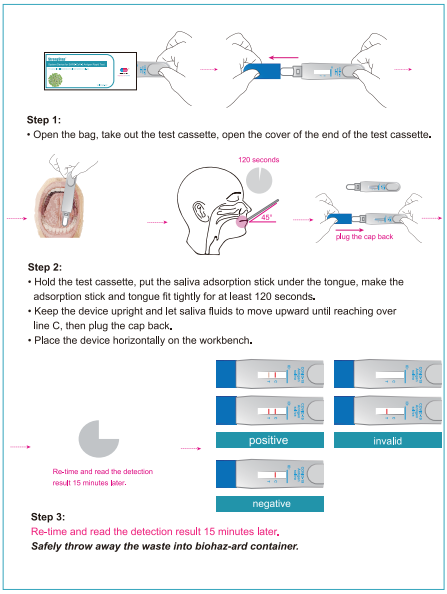
Passaggio 1:
Apri la borsa, elimina il dispositivo di prova, apri la copertura della fine del dispositivo di prova.
Passaggio 2:
• Tenere la cassetta di perbosciera, mettere la stick di adsorbimento della saliva sotto la lingua, fare bene la levetta di adsorbimento e la lingua per almeno 120 secondi.
• Mantieni il dispositivo in posizione verticale e lascia che i fluidi della saliva si muovano verso l'alto fino a raggiungere la linea C, quindi collega il tappo.
• Posizionare il dispositivo in orizzontale sul banco di lavoro.
Passaggio 3:
Rifronta e leggi il rilevamento resuh 15 minuti dopo.
Getta in modo sicuro i rifiuti nel contenitore Biohaz-AD.
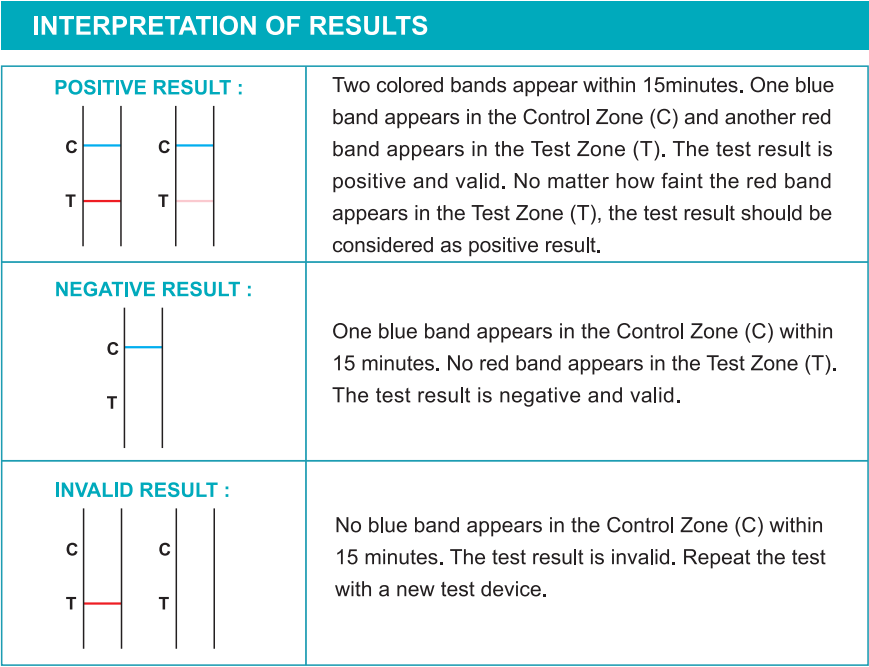
Controllo di qualità
I controlli procedurali interni sono inclusi nel test. Una banda blu che appare nella regione di controllo (C) è considerata un controllo procedurale interno. Conferma il volume del campione sufficiente e la corretta tecnica procedurale.
Limitazioni del test
1. Il kit è destinato a utilizzare per il rilevamento qualitativo di antigeni SARS-CoV-2 dalla saliva.
2. Questo test rileva SARS-CoV-2 sia vitali (live) che non vitali. Le prestazioni del test dipendono dalla quantità di virus (antigene) nel campione e possono o meno correlarsi con i risultati della coltura virale eseguiti sullo stesso campione.
3
4. La mancata seguizione della procedura di prova può influire negativamente sulle prestazioni del test e/o invalidare il risultato del test.
5. Il kit è solo per lo screening presuntivo. I risultati negativi non escludono l'infezione da SAR-COV-2 e la persona non è contagiosa. Se sono presenti sintomi, cercare ulteriori test immediati.
6. I risultati dei test devono essere correlati con la storia clinica, i dati epidemiologici e altri dati disponibili per il medico che valuta il paziente.
7. I risultati dei test positivi non escludono le co-infezioni con altri agenti patogeni e non possono necessariamente determinare se una persona è contagiosa.
8. I risultati dei test negativi non hanno lo scopo di governare in altre infezioni virali o batteriche non SARS.
9. I risultati negativi dei pazienti con sintomo devono essere trattati come presuntivi e confermati con un test molecolare autorizzato dalla FDA locale, se necessario, per la gestione clinica, incluso il controllo delle infezioni.
10. Le raccomandazioni sulla stabilità dei campioni si basano su dati di stabilità dei test e le prestazioni dell'influenza possono essere diverse con SARS-CoV-2. Gli utenti devono testare i campioni il più rapidamente possibile dopo la raccolta dei campioni.
11. La sensibilità per il test RT-PCR nella diagnosi di Covid-19 è solo del 50% -80% a causa della scarsa qualità del campione o del punto temporale della malattia nella fase RecoverD, ecc. inferiore a causa della sua metodologia.
12. I valori predittivi positivi e negativi dipendono fortemente dai tassi di prevalenza.
I risultati dei test positivi hanno maggiori probabilità di rappresentare risultati falsi positivi durante i periodi di attività SARS-COV-2 poca / no quando la prevalenza della malattia è bassa. I risultati dei test negativi sono più probabili quando la prevalenza della malattia causata dalla SARS-CoV-2 è elevata.
13. Gli anticorpi monoclonali possono non riuscire a rilevare o rilevare con meno sensibilità, virus dell'influenza SARS-COV-2 che hanno subito piccoli cambiamenti di aminoacidi nella regione dell'epitopo bersaglio.
14. Le prestazioni di questo test non sono state valutate per l'uso in pazienti senza segni e sintomi di infezione respiratoria e prestazioni possono differire negli individui asintomatici.
15. La quantità di antigene in un campione può diminuire all'aumentare della durata della malattia.
I campioni raccolti dopo il giorno 7 di malattia hanno maggiori probabilità di essere negativi rispetto a un test RT-PCR.
È noto che la sensibilità del test dopo i sette giorni di insorgenza dei sintomi diminuisce rispetto a un test RT-PCR.
16. Non è consigliabile utilizzare il campione VTM (Virus Transportation Media) in questo test, se i clienti insistono per utilizzare questo tipo di campione, i clienti dovrebbero convalidare se stessi.
17. Sono necessari test frequenti per aumentare la sensibilità della diagnosi di Covid-19.
18. Nessun abbandono di sensibilità rispetto al tipo selvaggio rispetto alle seguenti varianti -b.1.1.7; B.1.351; B.1.2; B.1.1.28; B.1.617; B.1.1.529.
19. Risultati positivi indicano che gli antigeni virali sono stati rilevati nel campione prelevato, si prega di autoavagliazione e informare prontamente il medico di famiglia e/o il tuo dipartimento sanitario locale in conformità con i requisiti statali.
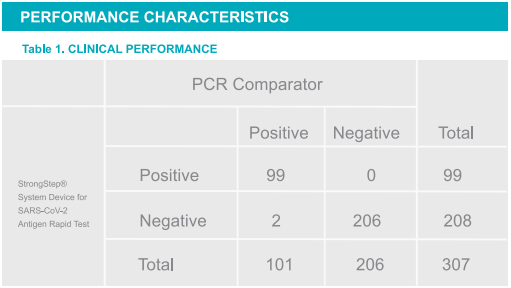
Accordo percentuale positivo: (PPA) = 98,02%(93,03%~ 99,76%)*
Accordo percentuale negativo: (NPA) = 100%(98,23%~ 100%)*
Tasso di coincidenza totale = 98,76%
*Intervallo di confidenza al 95%
Prestazioni analitiche
a) Limite di rilevamento (LOD):
Il limite di rilevamento (LOD) del test è stato determinato utilizzando diluizioni limitanti di SARS-CoV-2 inattivate. È una preparazione di coronavirus-2 correlato alla SARS (SARS-CoV-2), che si isola in Cina CDC, che è stato inattivato dal β-propiolattone. Il materiale è stato fornito congelato a una concentrazione di TCID50di 5,00 x105/ml.
Per determinare la SARS-CoV-2 per riflettere il test quando si utilizza la saliva diretta. In questo studio circa 50 μl della diluizione del virus è stato aumentato con il campione negativo della saliva.
Il LOD è stato determinato in tre passaggi:
1. Screening LOD
Le diluizioni di 10 volte del virus inattivato sono state realizzate in saliva negativa ed elaborate per ogni studio come descritto sopra. Queste diluizioni sono state testate in triplicato. La concentrazione che dimostrava 3 su 3 positive è stata scelta per la ricerca della gamma LOD.
2. LAD Range Reperti
Sono state fatte cinque (5) diluizioni di raddoppio del TCID50di 5,00 x102/ml Concentrazione nella saliva negativa elaborata per lo studio come descritto sopra. Queste diluizioni sono state testate in triplicato. La concentrazione che dimostra 3 su 3 positivi è stata scelta per la conferma LOD.
3. Conferma LOD
La concentrazione TCID50di 2,50 x102/ml diluizione è stata testata per un totale di venti (20) risultati. Almeno diciannove (19) risultati di venti (20) sono stati positivi.
Conclusione:
Sulla base di questo test, la concentrazione è stata confermata come:
LOD: TCID502,50 x102/ml
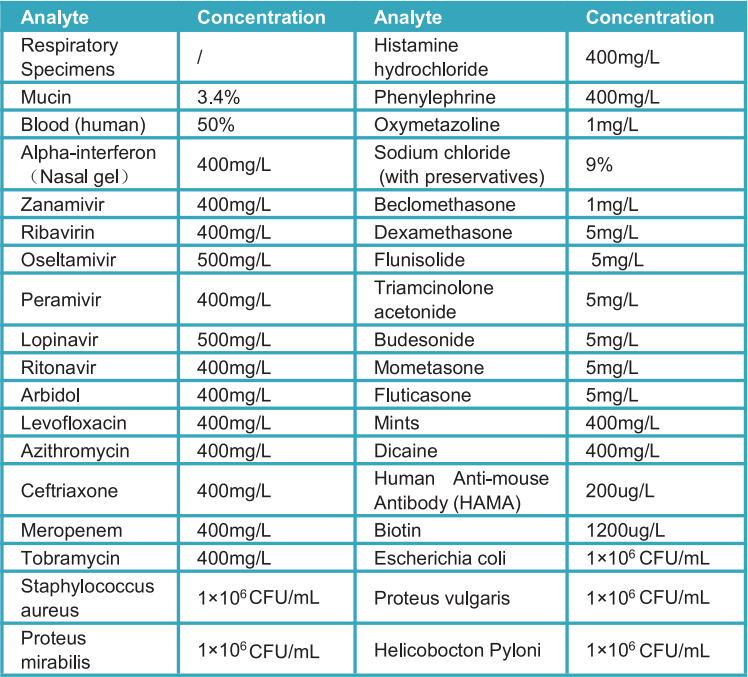
b) reattività incrociata:
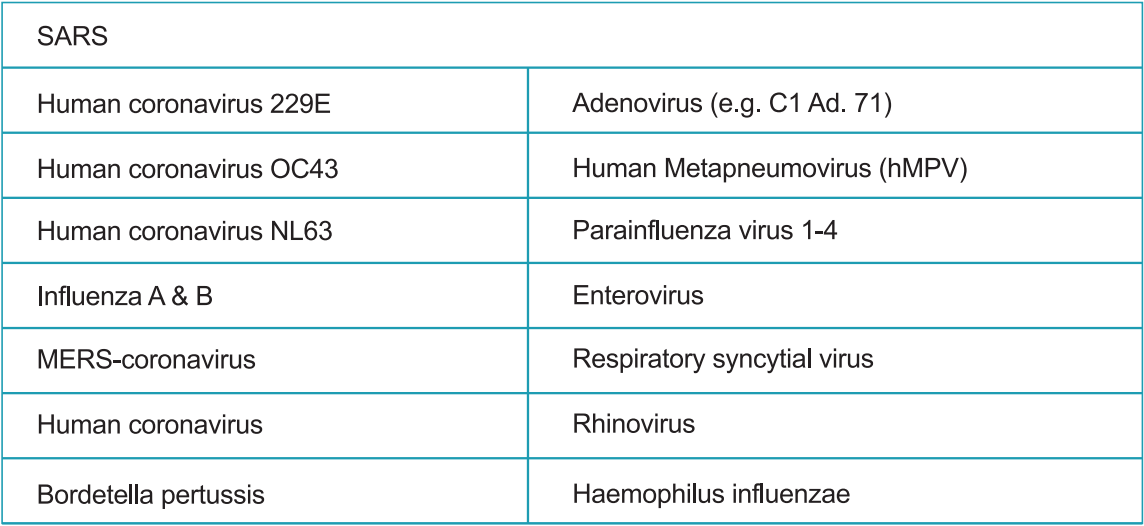
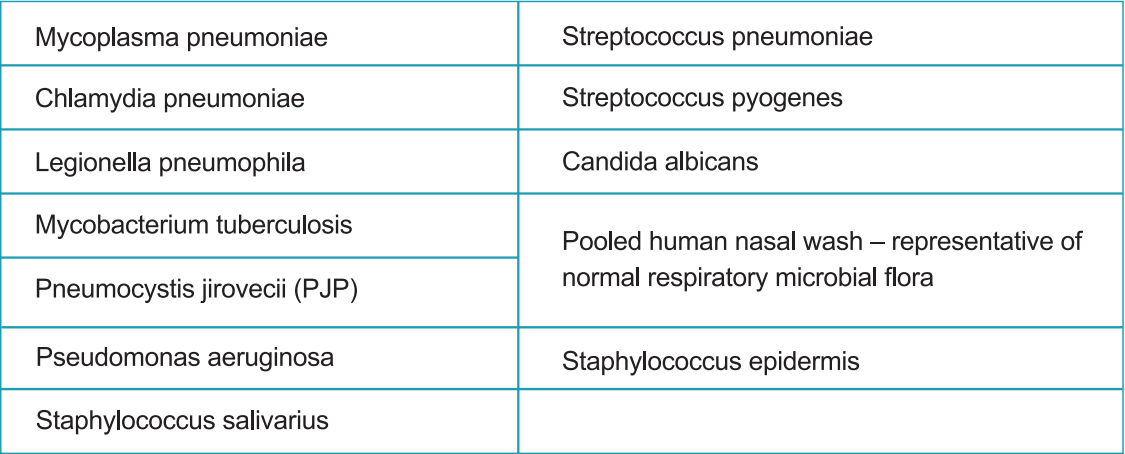
La reattività incrociata del dispositivo di sistema Strongstep® SARS-COV-2 ANtigene Rapid Test è stato valutato testando vari microrganismi (10⁶ CFU/mL), virus (10⁵ PFU/mL) e matrici negative che possono potenzialmente reactare con il Strongstep® Dispositivo di sistema Test rapido dell'antigene SARS-2.
Ogni organismo e virus sono stati testati in triplicato. Sulla base dei dati generati da questo studio, il dispositivo di sistema Strongstep® per il test rapido dell'antigene SARS-CoV-2 non reagisce incrociato con gli organismi o i virus testati.
c) interferire la sostanza:
Le potenziali sostanze interferenti del test rapido dell'antigene SIRSTeP® SARSTSTEP® sono state valutate testando varie sostanze con concentrazione al di sotto che potrebbero potenzialmente interferire con il test rapido dell'antigene SIRSTEP® SARS-2. Ogni sostanza è stata testata in triplicato. Sulla base dei dati generati da questo studio, il test rapido dell'antigene Strongstep® SARS-CoV-2 non interferisce con le sostanze testate.
d) Effetto gancio
La più alta concentrazione di stock SARS-CoV-2 inattivato dal calore disponibile (TCID50di 5,00 x 105/ml) è stato testato. Non è stato rilevato alcun effetto hook.




1人份抗原卡实物图唾液版1_00_副本-300x216.png)